-
Montage distillation simple
Distillation SIMPLE
Distilation FRACTIONNEE
Télécharger « 4_TECH_distil_reduite.swf »
Fiche METHODE distillation fractionnée
 votre commentaire
votre commentaire
-
Montage chauffage à reflux avec ampoule de coulée
Montage chauffage à reflux avec colonne CaCl2
Fiche METHODE
 votre commentaire
votre commentaire
-
Montage de Dean-Stark
Principe : La réaction d'estérification produit de l'eau,
qui, extraite du mélange, empêche la réaction inverse et augmente ainsi le rendement en déplaçant l'équilibre vers la droite.L'ajout de cyclohexane permet de créer un azéotrope dont la température d'ébullition
est inférieure aux composés. Le mélange ( eau-cyclohexane ) évaporé, condensé dans le réfrigérant, tombe dans le Dean-stark . L'eau plus dense, constitue la phase inférieure , le cyclohexane en excès retourne dans le ballon ( mélange réactionnel )Principehttps://www.thinglink.com/scene/901818883717988356
Vidéo
Exercices corrigés
http://www.chimix.com/an12/bac12/usa3.html
Attention à :
-remplir le Dean-stark jusqu'en haut pour ne pas appauvrir en cyclohexane le milieu réactionnel
 1 commentaire
1 commentaire
-
-
-
Doc
« Spectres de carbone 13.docx »
« Spectres de carbone 13.pdf »
Animation
Vidéos
Pour approfondir
 votre commentaire
votre commentaire
-
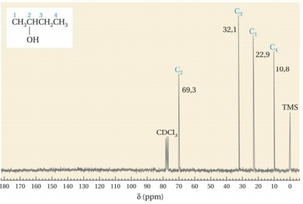
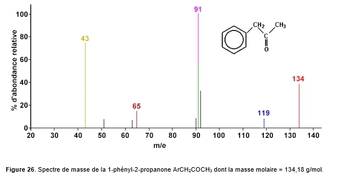
Spectrométrie de masse
C’est l’étude de la masse des espèces atomique qui renseigne sur la nature, la composition et la structure.
Le composé est ionisé. Les espèces porteuses de charge électriques qui en résultent sont soumises à l’action d’un champ électrique et/ou magnétique.
L’étude des trajectoires suivies (dans une enceinte sous vide) permet de déterminer le rapport masse/charge des ions, donc leurs natures.
Le spectre de masse représente l’abondance statistique de chaque type d’ion formé suivant son rapport masse/charge
Dans un spectromètre de masse, les principales étapes sont : ionisation, accélération, séparation (en fonction de m/z) et détection.Un couplage très utilisé est la chromatographie/SM.
La sortie de la colonne est reliée par l’intermédiaire d’une interface à un spectromètre de masse.
On trace le chromatogramme en courant ionique total (TIC).la sélection d’ion (mode SIM) permet de faire de l’analyse quantitative.https://pca.ujf-grenoble.fr/techniques-d-analyses/spectrometrie
Doc
Animation
Vidéo
Pour approfondir
 votre commentaire
votre commentaire
-
Évaporateur rotatifPrincipe de l’ Évaporateur rotatif
Cet appareil permet d’éliminer rapidement un solvant volatil par évaporation d'un hétéroazéothrope..
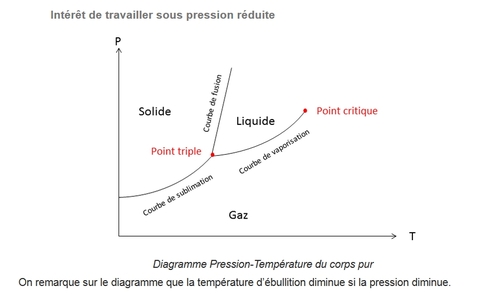
Le principe est basé sur l’abaissement du point d’ébullition avec la pression.Doc
en Images
« fiche_evaporateur_rotatif.pdf »
Image interactive
Les étapes d'utilisation de l'évaporateur rotatif.
- Mettre le thermostat du bain en route. La température sera adaptée au solvant à extraire.
- Mettre l’eau dans la colonne de condensation
- Déclencher la trompe à eau (robinet au maximum de son débit).
- Placer le ballon contenant la solution à purifier de son solvant. Le fixer par sécurité par une pince .
- Fermer le robinet .
- Mettre le ballon en rotation . On va généralement d'autant plus vite que le bain est plus chaud.
- Descendre le ballon pour le mettre en contact avec la solution : le ballon doit juste "lécher" le bain.
- Attendre les premières gouttes de solvant dans le ballon de recueillement (parfois ces vapeurs n'apparaissent pas, elles ne sont condensées et sont entraînées directement dans la pompe à eau).
- Vérifier que le solvant est distillé : le ballon doit être froid.
- Arrêter le tout en prenant garde de ne pas faire un retour d'eau en coupant la trompe à eau en premier : commencer par ouvrir le robinet (8), enlever la pince et récupérer le ballon, fermer le robinet de la trompe à eau et éteindre l'appareil.
Fiche METHODE
 votre commentaire
votre commentaire
-
Résonance Magnétique Nucléaire (disponible à proximité de la plateforme)
Donne la structure des composés moléculaire organique.
La RMN tire des informations de l’interaction qui naît entre les noyaux des atomes de certains éléments présents dans l’échantillon et le champ magnétique intense et constant, produit par un aimant auquel on le soumet (signaux de résonance).
Sur un appareil, on donne la fréquence nominal du proton qui est lié au champ de l’appareil (exemple B0=9T entraîne 1H=400MHz)
Le spectre RMN correspond à l’absorption, par certain atome de l’échantillon, de certaines des fréquences présentent dans la source électromagnétique.
De l’interprétation de ces signaux (position, aspect, intensité) on en déduit la structure.
Cette technique fait appelle au spin des noyaux qui permet d’expliquer le comportement des atomes dans un milieu où il règne une direction privilégiée.
Il ne faut donc pas de spin nul pour étudier un atome en RMN
Il ne faut donc pas que A (nucléon) et Z (proton) soient tous deux paire, sinon il n’y a pas de spin (donc pas de RMN)
Donc pas de RMN pour par exemple C (A=12, Z=6) ; Hé (A=4, Z=2) ; O (16, 8) ; Si (28, 14) ; S (32, 16)…
Cependant la sensibilité varie suivant les noyaux.Source : https://pca.ujf-grenoble.fr/techniques-d-analyses/spectrometrie
http://www.web-sciences.com/documents/terminale/tedo06/teco06.php
Fiche méthode
http://btsmetiersdelachimie.eklablog.com/calcul-de-deplacement-a129834054
DIAPORAMA
https://drive.google.com/file/d/0B0oodXbnZPW6Y0xlSENJOXlqYkU/view?usp=sharing
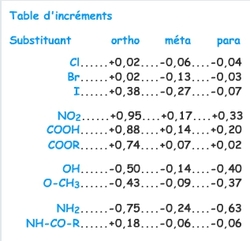
Calcul de déplacements chimiques à partir de tables d'incréments
http://uel.unisciel.fr/chimie/spectro/spectro_ch03/co/apprendre_ch3_56.html
http://www.unice.fr/cdiec/cours/rmn_web/rmn_couplages/cs17a.htm
Courbe d'intégration
http://www.unice.fr/cdiec/cours/rmn_web/rmn_delta/c_delta.htm
http://uel.unisciel.fr/chimie/spectro/spectro_ch03/co/apprendre_ch3_21.html
Table de données
« Table de données SPECTROSCOPIE DE RMN DU PROTON.docx »
ou sur les sites
http://www.chem.wisc.edu/areas/reich/nmr/h-data/hdata.htm
http://www.unice.fr/cdiec/cours/rmn_web/tables/c_tables.htm
Vidéos
Sites :
http://uel.unisciel.fr/chimie/spectro/spectro_ch03/co/apprendre_ch3_56.html
http://www.web-sciences.com/documents/terminale/tedo06/teco06.php
Une Aide VIRTUELLE ?

http://mirage.ticedu.fr/?p=2673
 votre commentaire
votre commentaire
-
MACRO WORD VERRERIE
Une fois ouvert, un menu dans Compléments apparait dans Word
pour intégrer de nombreux schémas en Chimie votre commentaire
votre commentaire
-
L’HPLC en 12 étapes
Un cours complet :
http://www.perrin33.com/biochanalys/chromato/chainelc_1.php
http://www.perrin33.com/biochanalys/chromato/lc-modseparations_1.php
Schéma de fonctionnement
Photos des équipements du BTS des métiers de la Chimie
Pompes et éluant et Analyseur
Boucle d'injection et Colonne ( polaire ou apolaire selon l'étude )
Boucle d'injection
Embout de l'injecteur
Positions Load pour "Remplir la boucle" à l'aide d'une seringue rincée 3 fois jusqu'à l'apparition d'une goutte sortante
et
Abaisser dans le position Injection pour "injecter" dans la boucle et commencer l'analyse...http://forums.futura-sciences.com/chimie/429345-colonne-c18-normal-inversee.html
Exemple de TP sur la Vanille
http://www.asso-etud.unige.ch/aecb/rapports/3eme/chianalytique/hplc_04.pdf
 votre commentaire
votre commentaire
-
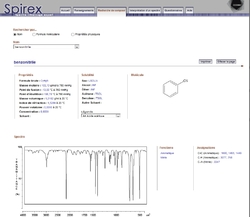
Générateur de spectres IR, RMN, C13, H
SDBS
http://sdbs.db.aist.go.jp/sdbs/cgi-bin/direct_frame_top.cgi
 votre commentaire
votre commentaire
-
SPECTRES Infra-ROUGE
http://brussels-scientific.com/?p=6159
http://www.web-sciences.com/documents/terminale/tedo05/teco05.php
Dépot d'une goutte de solution sur la cellule du Spectro IR
Manipulation
Faire attention à :
- Nettoyer la cellule à l'aide d'un coton imbibé l'éthanol
- Faire le Back Ground ( ne pas trop parler ..... CO2 et H20 captés)
- Déposer une goutte sur le support ou directement sur la cellule une micro spatule de composé solide
Principe
http://brussels-scientific.com/?p=6159
http://mathias.borella.fr/2-1-La-spectroscopie-infrarouge.html
Table de données IR
Principe du Spectromètre IR

Brochure IRaffinity 1

Vidéo
Une aide VIRTUELLE ? avec MIRAGE

http://mirage.ticedu.fr/?p=2670
 votre commentaire
votre commentaire
-
Contactez le Lycée : 04 74 53 00 13
Site du Lycée : http://www.ac-grenoble.fr/lycee/galilee.vienne/pages/BTS%20MC.php
Contactez le Responsable du Site : dimpondy@gmail.com
JACQUIER-ROUX Dimitri,
Intervenant en TP de chimie de Synthèse
BTS des Métiers de la Chimie
Vienne, Isère
 votre commentaire
votre commentaire
-
Montage
Révélation sous lampe UV
Les systèmes conjugués de moins de huit doubles liaisons conjuguées absorbent uniquement dans les ultraviolets ( 254 nm ) et apparaissent incolores à l'œil humain
Une révélation sous UV est nécessaire !
Attention à :
-ne pas confondre éluant et solvant
-à choisir les correctement les composés à éluer.
-utiliser un tube capillaire pour chaque dépôt
-à saturer votre cuve qq minutes avant avec papier buvard ( plus rapide )
-à ce que le niveau d'éluant soit plus bas que la ligne de dépôt
-à marquer le front de l'éluant
è noter les différents composés ( brut, pur, commercial,..)
Fiche METHODE
 votre commentaire
votre commentaire
-
Matériel pour détermination du point de Fusion d'un composé solide
Détermination de Tf
Lecture de Tf
On peut lire T fus : 168 °C
Étalons pour étalonner le Bac
Faire attention à :
-l'allumer 1 h avant
-à nettoyer à l'alcool+coton le banc
( Si T fus inconnue : Prendre le composé et déterminer rapidement sa T fus )
-à l'étalonner avec un étalon de T fus. inf = T fus. du composé +/- 2°C à +/-5 °C
-à déterminer avec précision Tf
-à nettoyer le banc après utilisation
Fiche METHODE
 votre commentaire
votre commentaire
-
-
Règle : Les résultats ne sont jamais plus précis
que la moins précise des données !Ecriture scientifique et Nombre de chiffres significatifs
Exercices interactifs : Testez-vous !
https://www.ac-grenoble.fr/disciplines/spc/file/accompa/chiffres/co/Module_seq_1.html
 votre commentaire
votre commentaire
-
Le composé à purifier doit être insoluble à froid et soluble à chaud dans le solvant
Le solvant de recristallisation doit :
- ne pas réagir avec le produit à purifier
- ne pas dissoudre les impuretés à chaud ET à froid
- avoir un point d’ébullition le plus bas possible
- être le moins toxique possible
En général, une recherche du solvant de recristallisation se conduit de la manière suivante :
- Dissoudre le composé à chaud dans un minimum d'un solvant A dans lequel le composé soit très soluble,
- Ajouter, à chaud toujours, par quantités successives, suffisamment d'un solvant B, dans lequel le composé est très peu soluble, de manière à obtenir un début de précipitation du composé à purifier, à chaud,
- Ajuster avec la quantité juste suffisante de solvant A pour obtenir la redissolution à chaud du composé à purifier dans le mélange.
Télécharger « 12_TECH_recristallisation.swf »
Sitographie
http://www.zysman-colman.com/courses/chm302/Recristallisation%20et%20temperature%20de%20fusion.pdf
Fiche METHODE
Cristallisation
 votre commentaire
votre commentaire
-
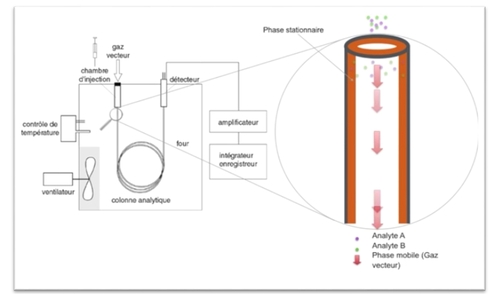
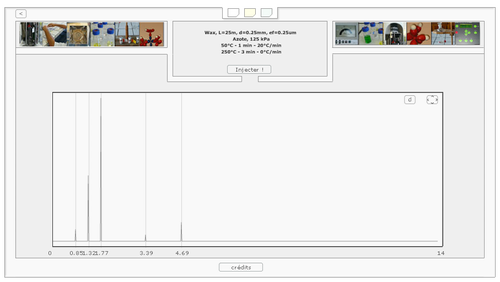
Chromatographie en Phase Gazeuse
Télécharger « 5989-6159FR.pdf »
Facade de la CPG
Colonne de CPG
http://www.sciences-en-ligne.com/DIST/Data/Ressources/lic2/chimie/chi_exp/chromatographie/cpg.htm
http://www.lachimie.fr/analytique/chromatographie/index.php
et toutes le fiches afférentes à la CPG
http://www.lachimie.fr/analytique/chromatographie/plan.php
ou
http://jflemen.iutlan.univ-rennes1.fr/CHIMIE/Chimie1/CHROMATO.HTM
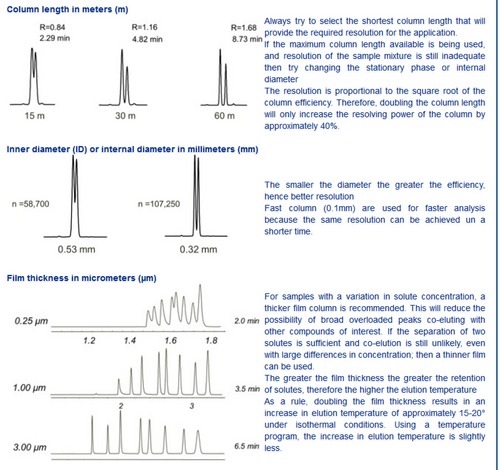
Source : http://www.interchim.com/pp/620/technical-information.html
 votre commentaire
votre commentaire
-
Méthode et précautions expérimentales
Principes généraux
http://formalabo.insa-rennes.fr/media/technique/10_TECH_chromatographie.swf
http://www.123bio.net/cours/index.html
https://www.memoireonline.com/01/09/1898/m_Caracterisation-Dun--Colorant--Naturel1.html
Analyse des composant du thé de chine
http://www.puerh.fr/article/science_sante_vers_une_empreinte_des_thes_puerh.htm
Analyse des composant du Paprika
http://www.maxicours.com/se/fiche/2/5/381725.html
Analyse des chlorophylles et xanthophylle
Dossier très complet sur
http://www.snv.jussieu.fr/bmedia/Photosynthese/exp21.html
http://wiki.scienceamusante.net/index.php?title=La_chlorophylle
https://fr.scribd.com/document/121964481/Botany-for-the-Artist
Séparations des colorants d'un sirop de menthe
 votre commentaire
votre commentaire
-
Appareil de Mesure de Point de Fusion analogique - SMP11le Totolli
Descriptif :
-L'échantillon à tester est placé dans un tube capillaire et inséré directement dans le bloc de chauffage.
-La température s'élève rapidement (20 °C/min) ou plus lentement (réglage manuel entre 1 et 10 °C/min) jusqu'à
la température de fusion.
-Les échantillons sont éclairés par une LED et visualisés à l'aide d'une lentille grossissante facile à nettoyer.Fiche méthode
Notices d'utilisation
http://www.batailler-labo.fr/art?id=1181
 votre commentaire
votre commentaire
-
-
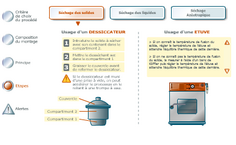
Les agents désséchants
Afin d'éliminer les traces d'eau de solvants ou réactifs, ou à la fin d'une synthèse, on peut utiliser divers agents desséchants plus ou moins efficaces et recommandés selon le produit à sécher. Un desséchant doit avoir les caractéristiques suivantes :
- Ne pas réagir avec la substance à sécher.
- Capter le plus possible les traces d'eau.
- Agir rapidement.
- Se séparer facilement de la substance à sécher.
http://wiki.scienceamusante.net/index.php?title=Agents_dess%C3%A9chants
 votre commentaire
votre commentaire
-
Soap film flowmeter pour CPG
Made of borosilicate glass, these soap film bubble flowmeters are used in routine
analytical laboratory gas chromatography to measure flow rate of the carrier gas.
A soap bubble, formed in the bottom of the graduated tube, is pushed upward by gas from
exit end of the chromatograph. Flow rate is determined by measurement of
the volume through which the bubble travels in a definite period of timeYou can
https://www.thomassci.com/Instruments/Flowmeters/_/Soap-Film-Flowmeters
 votre commentaire
votre commentaire
-
Simulateurs en HPLC et GC
ou sur
http://master-analyse-controle-inscription.univ-lyon1.fr/GCSimul.asp
 votre commentaire
votre commentaire